Script: http://www.tulane.edu/~wiser/protozoology/notes/intes.html#giardia
| Lumen élő protozoonok |
|---|
Ostorosok:
Ameba:
Elemi:
Microsporidium:
Más:
|
Számos protozoonok él a gyomor-bél traktus emberben (lásd a keretben). Ez a lista magában foglalja a képviselők számos különböző egysejtű csoportok. A legtöbb ilyen protozoa nem patogén kommenzális, vagy csak eredményez enyhe betegség. Néhány ilyen organizmusok okozhat súlyos betegség bizonyos körülmények között. Például, a Giardia lamblia okozhat súlyos akut hasmenés, ami ahhoz vezethet, hogy egy krónikus hasmenés és táplálkozási rendellenességek; Entamoeba histolytica válhat erősen virulens és invazív szervezet, amelynek következtében a potenciálisan halálos szisztémás betegség. Elemi és microsporidium fajok (máshol tárgyaljuk), amelyek rendszerint nem váltanak ki súlyos betegség, okozhat súlyos, életveszélyes hasmenést AIDS betegek és más immunhiányos egyének. Trichomonas vaginalis nem lakik a gyomor-bél traktusban, de gyakran felmerül a bél ostorosok. Ez fertőz az urogenitális traktus és okoz egy szexuális úton terjedő betegség.
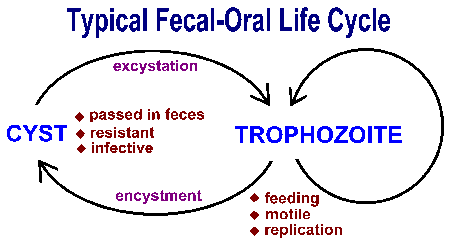
A bél protozoonok továbbítják a széklet-szájon és hajlamosak mutatnak hasonló az életciklusa, amely egy ciszta színpad és a színpadi trophozoite (ábra). Fekális-orális átvitel magában foglalja a lenyelése élelmiszer vagy víz szennyezett ciszták. Miután lenyelés megfelelő gazdasejt által, a ciszták átalakulni trophozoiták amely mutatnak aktív metabolizmus és általában mozgékony. A parazita veszi fel a tápanyagokat és megy ivartalan replikáció során a táplálkozási fázis. Néhány trophozoiták alakul át ciszták helyett átesett replikáció. Ciszták jellemzi ellenálló fal és kiválasztódnak a széklettel. A ciszta fala funkciókat, hogy megvédje a szervezetet a kiszáradástól a külső környezet, mint a parazita megy viszonylag nyugalmi időszak vár, hogy elfogyasszák a következő gazda. Tényezők, amelyek növelik a valószínűségét elfogyasztásának szennyezett anyagok székletanyag szerepet játszanak az átviteli ennek intestinalis protozoa (lásd a keretben). Általában helyzetekben megvalósuló szoros ember-ember kapcsolat és unhygenic feltételek segítik elő adást.
rossz személyi higiéniai
fejlődő országok
vízbázisú járványok
férfi homoszexualitás
zoonózis?
|
TÉMÁK:
• Giardiasis
· Életciklus és morfológia
– Trophozoite
– Hólyag
· Az ragasztóanyag korong
· Tünetek és patogenezise
· Diagnózis
· Kezelés és ellenőrzés
• Trichomoniasis
• Dientamoeba fragilis
• Balantidosis
• Amebiasis
• Blastocystis hominis
• Nem patogén kommenzális
GIARDIASIS
Giardia lamblia (más néven G. duodenalis, lásd megjegyzések taxonómia) egy protozoon parazita, amely colonizes felső részei a vékonybélben. Ez az egész világon elterjedt, és a leggyakoribb protozoa izolált emberi széklet. Az előfordulási becsült 200 millió klinikai eset évente. Sőt, valószínűleg ez volt az első szimbiotikus egysejtű valaha megfigyelt. Elég valószínű, hogy Van Leeuwenhoek, a feltaláló a mikroszkóp, amelyet először Giardia a 1681in saját széklet alapján a leírás jellegzetes mozgást. Azonban van Leeuwenhoek soha beküldött rajz az élőlények és Lambl általában adott hitel azonosítására Giardia a székletben a gyermekgyógyászati betegek Praque 1859.
Jellemzően Giardia nem invazív és gyakran tünetmentes fertőzéseket. Tüneti giardiasisnak jellemzi akut vagy krónikus hasmenés és/vagy más gyomor-bélrendszeri megnyilvánulásai.
ÉLETCIKLUS ÉS MORFOLÓGIA
Giardia mutat egy tipikus fekális-orális átvitel ciklus (lásd fent). A fertőzés során szerzett lenyelése ciszták. Tényezők szennyezését okozó élelmiszer vagy víz széklet korrelálnak sebességváltó (doboz). Például Giardiasis különösen gyakori a gyermekek és különösen a gyermekek intézmények vagy napközi. A fejlődő országokban a rossz higiéniai hozzájárul a magasabb szintű giardiasisnak és víz-eredetű megbetegedések oka a nem megfelelő vízkezelés is dokumentáltak. Backpackers területeken nem emberi település vélhetően megszerzi iszik patakok és egyes adatok arra utalnak, hogy a hódok a tározó. Azonban a zoonózis továbbítása Giardia ellentmondásos, és nem egyértelműen bizonyított. Nem világos, hogy a Giardia lamblia jelent egyetlen faj képes megfertőzni sokféle állat, vagy minden gépnek van saját “pet” Giardia. Bizonyíték arra, hogy a Giardia közötti átvitel kutyák és az emberek meglehetősen ritka előnyben részesíti. Molekuláris bizonyítékok arra utalnak, hogy egyes izolátumok mutatnak szűk befogadó tartományokban, míg mások mutatnak széles befogadó tartományban (lásd megjegyzések taxonómia). Függetlenül attól, hogy a zoonózis lehetséges az átvitel, személy-személy átvitel a legelterjedtebb átviteli mód és a kockázati tényezők szoros emberi kapcsolat együtt higiénikus körülmények között.
A lenyelt ciszta halad át a gyomron, és excystation zajlik a nyombélben. Excystation lehet indukálni in vitro egy rövid idejű expozíció a ciszták, hogy savas pH (~ 2), vagy más források a hidrogén-ionokat. Ez a kitettség a savas pH utánozza a feltételeket, a gyomor és valószínűleg funkcionál, mint környezeti Cue a parazita. Ostoros tevékenység megkezdése 5-10 percen belül követi a savas kezelés és a trophozoite bukkan egy kis szünetet a ciszta fala. A bontás a ciszta fala úgy véljük, hogy közvetíti a proteázok. A trophozoite vetik alá, citokinézis (sejtosztódás nélkül nukleáris replikáció) után 30 percen belül új a ciszta ami a két binucleated trophozoiták.
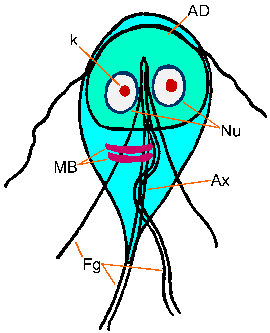 A Giardia trophozoite mutat jellegzetes körte, vagy könnycsepp, alakja kétoldali szimmetria, ha felülről nézve (ábra). Ez tipikusan 12-15 lm hosszú, 5-10 lm széles, és 2-4 lm vastag. Jellegzetessége a festett trophozoite tartalmazza: két mag (Nu) központi karyosomes (K), rostszálak fut a hossza a parazita, és a medián szervek (MB). A nagy karyosome és nem a perifériás kromatin ad a magok egy halo megjelenést. A fibrillák nevezzük axonemes (AX) és van kialakítva a proximális régióban a csillók (Fg) belül a test a trophozoite. A medián testek egy pár ívelt rúd alakú szerkezetek, amelyek ellen posterior a magok. Ultrastrukturális szinten a medián szervek tartalmaznak egy sor mikrotubulusok. A funkció a medián szervek nem ismert, de a legtöbb azt hiszik, hogy valamilyen módon részt a ragasztóval lemez és kialakulását. Egy ragasztó lemez (AD), nem mindig látható fénymikroszkóppal, elfoglalja a ventrális oldalán az elülső végén.
A Giardia trophozoite mutat jellegzetes körte, vagy könnycsepp, alakja kétoldali szimmetria, ha felülről nézve (ábra). Ez tipikusan 12-15 lm hosszú, 5-10 lm széles, és 2-4 lm vastag. Jellegzetessége a festett trophozoite tartalmazza: két mag (Nu) központi karyosomes (K), rostszálak fut a hossza a parazita, és a medián szervek (MB). A nagy karyosome és nem a perifériás kromatin ad a magok egy halo megjelenést. A fibrillák nevezzük axonemes (AX) és van kialakítva a proximális régióban a csillók (Fg) belül a test a trophozoite. A medián testek egy pár ívelt rúd alakú szerkezetek, amelyek ellen posterior a magok. Ultrastrukturális szinten a medián szervek tartalmaznak egy sor mikrotubulusok. A funkció a medián szervek nem ismert, de a legtöbb azt hiszik, hogy valamilyen módon részt a ragasztóval lemez és kialakulását. Egy ragasztó lemez (AD), nem mindig látható fénymikroszkóppal, elfoglalja a ventrális oldalán az elülső végén.
Giardia trophozoiták rendelkezik négy pár csillók, és rendkívül mozgékony. Három pár csillók, kilábalni a dorzális (elülső, hátsó-oldalsó, caudalis) és egy pár kilép a ventrális felszínén. Trophozoiták mutatnak jellegzetes kiszámíthatatlan csavaró mozdulattal, néha képest a csökkenő levél. Azonban a trophozoiták vannak túlnyomórészt csatolt hámsejtek a vékonybél (különösen a duodenumban és jejunumban), és ritkán található széklet, kivéve azokat az eseteket, súlyos hasmenés. Ez a kötődés az intesztinális epithelium közvetítik egy organellum a ventrális oldalán a parazita a továbbiakban a ragasztó lemez (lásd alább). A trophozoite elnyeli a tápanyagok a bélből keresztül pinocitózissal, és nem specializált etetés organellumok írtak le.
A trofikus szakaszban is jellemzi aszexuális replikáció. Mindkét magok osztani körülbelül ugyanabban az időben, és visszaállítja a citokinézishez binucleated állam. Minden lánya sejt kap egy példányt minden atommag. Mindkét magok jelennek egyenlő annak tekintetében, hogy a génexpresszió és egyéb tulajdonságait.
Alternatívaként a replikáció a trophozoite is encyst. Alatt encystment a parazita kerekíti, leválik a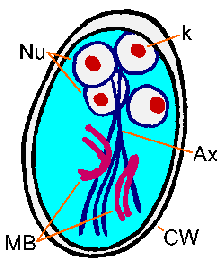 bélhámban, és titokban egy ciszta fala. Encystation is elvégezhető in vitro. Optimális indukció encystment nyerik megfosztja a trophozoiták epe pH = 7, majd egy magas koncentráció az epe pH = 7,8. A hiányzó epe semleges pH utánozza a feltételeket a nyálkahártya takaró szomszédos a bél epiteliális sejtekben, míg a magas koncentráció az epe több lúgos pH-analóg a bélrendszerben. Ezek a tanulmányok kiemelik, hogy milyen mértékben Giardia alkalmazkodott az élet a gyomor-bél traktusban.
bélhámban, és titokban egy ciszta fala. Encystation is elvégezhető in vitro. Optimális indukció encystment nyerik megfosztja a trophozoiták epe pH = 7, majd egy magas koncentráció az epe pH = 7,8. A hiányzó epe semleges pH utánozza a feltételeket a nyálkahártya takaró szomszédos a bél epiteliális sejtekben, míg a magas koncentráció az epe több lúgos pH-analóg a bélrendszerben. Ezek a tanulmányok kiemelik, hogy milyen mértékben Giardia alkalmazkodott az élet a gyomor-bél traktusban.
Molekuláris és elektronmikroszkópos vizsgálatokkal kimutatható szintéziséhez ciszta fala fehérjék és a megjelenése nagy szekréciós vezikulák a parazita citoplazmában kövesse az indukciós encystment. Miután ciszta fala kialakulása a paraziták megy egy kör nukleáris osztás nélkül citokinezist ami négy magok. Ez a négy magok (Nu) általában található az elülső végén a ciszta (ábra). A csillók, és a ragasztó lemezen elvész, mert a ciszta érlelődik, de a axonemes (Ax) és a medián szervek (MB) fennállnak. A jellegzetes fibrillák (azaz axonemes), amely kiterjeszti az egész hosszát a ciszta eredményez Giardia viszonylag könnyen egyértelmű azonosítására. A ciszták ovális alakú, és a tipikus intézkedés 11-14 pm hosszúságú és 6-10 um széles. Egyéb jellemzők Giardia ciszták közé tartozik a jól definiált fal (CW), amely gyakran félretesz a citoplazmából a parazita. A ciszták telt el a széklet, és túlélni, legfeljebb három hónapra megfelelő hőmérséklet és páratartalom esetén. Érett ciszták fertőző a következő gazda, ami történik lenyelik, így teljessé az életciklus.
AZ RAGASZTÓANYAG KORONG
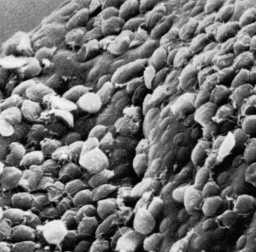
Egy egyedülálló ultrastruktúrális tulajdonsága Giardia a ragasztó lemez (más néven ventrális lemez, szopás lemez, balek, vagy harántcsíkolt lemez). A ragasztó lemez egy homorú szerkezet, amely elfoglalja mintegy kétharmadát az elülső végén a ventrális felszínén (ábra, bal panel). Ahogy a nevek jelenti, ez a struktúra szerepet játszik a mellékletet az trophozoite a bél epitélium és ultrastrukturális vizsgálatok kimutatják szoros összefüggést a ragasztó lemez és a bél kefeszegély (ábra, jobb felső panel). (Kattintson ide a nagyobb képhez.)
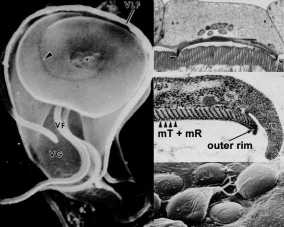
A fő összetevője a microribbons nevezett fehérjék giardins (aka béta-giardins). Ezek giardins játszanak elsősorban szerkezeti szerepet kialakulását a microribbons. Érdekes, hogy a giardins mutatják, hogy korlátozott homológiát nevű fehérje “harántcsíkolt szál assemblin” származó Chlamydomonas (a szabadon élő, bi-ostoros egysejtű algák). A Chlamydomonas Ez a fehérje fonalas szerkezetek tövénél a csillók. A giardins úgy fejlődött, hogy játszani egy másik funkcionális szerepet Giardia, de még kapcsolódó mikrotubulusok alapú citoszkeleton elemeit.
Ez az összefüggés a fehérjék részt vesznek a generációs összehúzó erő és más citoszkeletális elemek a ragasztó lemez azt sugallja, hogy kötődés által közvetített mechanikai erők által létrehozott parazita. Az a megfigyelés, hogy a lenyomatok és körkörös kupola alakú elváltozások maradnak a bél kefeszegélyének (azaz mikrobolyhokat) követően leválása trophozoiták (ábra, jobb alsó panel) összhangban áll a kontrakciós erő játszik szerepet mellékletet. Egyéb javasolt mechanizmusokat a mellékletet Giardia, hogy az intesztinális epithelium tartalmaznak hidrodinamikai erők által létrehozott ventrális csillók és a receptor által közvetített kötődését keresztül lektinek a trophozoite felületre. Azonban ostoros mozgás gyengén korrelál ragaszkodás és a felszíni lektinek fedezi a teljes trophozoite és nem kifejezetten lokalizálódik a ragasztó lemez.
TÜNETEK ÉS PATOGENEZISE
A klinikai tünetek járó Giardia fertőzés tartomány teljes látencia (azaz tünetmentes), az akut önálló megoldása hasmenés, krónikus szindrómák járó táplálkozási rendellenességek, fogyás és a kudarc gyarapodását. Gyermekek mutatnak klinikai tüneteket gyakrabban, hogy a felnőttek és a későbbi fertőzések általában kevésbé súlyosak, mint a kezdeti fertőzések. A lappangási idő általában 1-2 hét, de tartományok 1-75 napig nem számoltak be.
Az első jelei akut giardiasisnak émelygés, étvágytalanság, és a felső gyomor-bélrendszeri nyugtalanság. Ezek a jelek gyakran követi, vagy kíséri hirtelen fellépő robbanó, könnyező, bűzös hasmenés. Széklet járó Giardia fertőzés általában valamilyen laza, terjedelmes, habos és/vagy zsíros a hiánya vért vagy nyákot, amely segít megkülönböztetni giardiasisnak egyéb akut hasmenés. Egyéb emésztőrendszeri zavarok kapcsolódó giardiasisnak tartalmazza: felfúvódás, puffadás, étvágytalanság, görcsök és rossz kénsav böfögés (esetenként lila burbs). Az akut szakaszban rendszerint spontán 3-4 nap alatt, és gyakran nem ismerik el giardiasisnak. Esetenként azonban, az akut fertőzés továbbra is fennállnak, és vezet a felszívódási zavar, steatorrhea (túlzott mértékű csökkenése a zsír a széklettel), erőtlenség (erőtlenség) és a fogyás. Néhány akik megoldani a heveny tünetek nem egyértelmű a fertőzés, de lesz tünetmentes ciszta járókelők klinikai manifesztáció nélkül, míg mások esetleg néhány szórványos kiújulás az akut tünetek.
Akut fertőzés is kialakulhat a régóta tartó szubakut vagy krónikus fertőzés, ami ritkán évekig. A tipikus krónikus szakaszban betegnél ismétlődő rövid epizódok laza széklet fúj, amely lehet sárgás, habos és úszó kíséretében bél gurgulázó, hasi puffadás és felfúvódás. Az epizódok között a széklet általában pépes, de normális széklet vagy székrekedés is előfordulhat. Görcsök ritkák a krónikus fertőzés, de kénsav böfögés gyakori. Étvágytalanság, hányinger, gyomortáji és nyugtalanság van további gyakori panasz a krónikus fertőzések. A legtöbb krónikus esetben az élősködők és a tünetek spontán megszűnnek.
A konkrét mechanizmusok Giardia patogenezis hasmenéshez vezet és bélrendszeri felszívódási zavar még nem teljesen tisztázott, és nem specifikus virulencia faktorok azonosítottak. Felerősítése trophozoiták a kefeszegélyének lehetne előállítani mechanikai irritáció vagy károsodás. Ezen túlmenően, a normál villus szerkezet befolyásolja egyes betegeknél. Például villus tompító (atrófia) és kripta sejt hypertrophia és nőtt a kripta mélység észleltek különböző mértékben. A növekedés a kripta sejtek vezet újratelepítési az intesztinális epithelium által viszonylag éretlen enterocyták csökkentett abszorpciós kapacitással. A fokozott gyulladásos sejtes infiltráció a lamina propria is megfigyelték, és ez a gyulladás összefüggésben lehet a patológia. Giardia fertőzés is vezethet a laktáz-hiányban (lásd laktóz intolerancia alább), valamint más enzim hiányosságokat a microvilli. Ez a csökkentett emésztése és felszívódása oldott anyagok vezethet ozmotikus hasmenés és ez is magyarázza a felszívódási zavar szindrómák. Eddig egyetlen virulencia faktor vagy egységesítő mechanizmusát magyarázza patogenezise giardiasisnak. [Lásd még Kórélettana Hasmenés általános vita a hasmenés.]
Posta Giardia laktóz intolerancia. Egyes betegeknél a laktóz intolerence során aktív Giardia fertőzés, amely ezt követően is parazita kiürülését. Ez a klinikai megnyilvánulás miatt a parazita okozta laktáz hiányban és a leggyakoribb etnikai csoportok a hajlam a laktáz hiány. A laktáz egy enzim, amely lebontja a laktóz, a cukor a tejben, hogy a monoszacharidok, amely lehet felszívódik. Ez laktóz intolerence szindróma figyelembe kell venni a személyek, akik még jelen pépes széklet és fokozott gázképződés a kezelést követően, de nincs kimutatható paraziták.
DIAGNÓZIS
|
Parazita kimutatása |
Széklet vizsgálata
Duodenum Szívja vagy biopszia
|
Diagnózist megállapító ciszták vagy trophozoiták székletben vagy duodenojejunalis aspirátumokkal vagy biopsziát. Kimutatása a paraziták nehéz lehet, mivel Giardia nem jelenik meg következetesen a székletben minden betegnél. Egyes betegek magas szinten expresszálják a ciszták szinte minden a széklet, míg mások csak akkor mutatnak alacsony parazita rendbeli egyes széklet. Egy kevert minta, amelyben időszakok nagy ciszta kiválasztás váltakoznak időszakok alacsony kiválasztás, is megfigyelték. Ezen túlmenően, a paraziták könnyebb megtalálni az akut fertőzések, mint a krónikus fertőzések. Aspirációs biopszia és szintén nem erősíti meg a fertőzés miatt foltos loci fertőzés, és néhány kérdés hasznosságát ezen invazív eljárások.
Széklet vizsgálat az előnyben részesített módja Giardia diagnózist. Három széklet hozott időközönként legalább két nappal kell megvizsgálni. Vizes vagy laza széklet tartalmazhat mozgékony trophozoiták amelyek kimutatható a közvetlen vizsgálata nedves foltok. Ellenkező esetben a mintát meg kell őrizni, és foltos miatt trophozoite labilitás. A szívósabb ciszták viszonylag könnyen felismerhető, sem közvetlen, sem festett kenetek (lásd ciszta morfológia). Ezen túlmenően, diagnosztikai készletek alapján immunfluoreszcenciával vagy kimutatására Copro-antigének is rendelkezésre állnak.
Diagnózis is készítettek vizsgálata nyombélfekély folyadék trophozoiták. Duodenum folyadékot kapunk akár intubálás vagy Enterotest® (más néven “karakterlánc teszt”). A Enterotest® áll egy zselatin kapszula, amely egy nejlon húr a megfelelő hosszúságú. A szabad végét a húr van ragasztva a páciens arcát, és a kapszula lenyelése. Négy óra elteltével az egynapos string kerül beolvasásra, és az epe-festett nyál a távoli része a húr lekaparjuk, megvizsgálta mind a nedves tartó és állandó festéssel. A vékonybél-biopszia, lehetőleg több nyombél és jejunum oldalakat is felfedi trophozoiták csatolt bélhámban. [A vékonybél van osztva 3 szakaszból áll: a nyombél (az első vagy proximális rész után a gyomor); a jejunumban (a középső rész); és a csípőbélben (a disztális vagy utolsó részét, mielőtt a vastagbél).]
KEZELÉS ÉS ELLENŐRZÉS
A fertőzött egyének kell kezelni, mivel Giardia is fennállhat, és vezethet súlyos felszívódási zavar szindrómák és a fogyás. A kezelés hatékonyan csökkenti a morbiditást és nincsenek következmények. Metronidazol (Flagyl®), bár nem engedélyezett az Egyesült Államokban, giardiasisnak hatékonyan tisztítja a parazita (gyógyulási arányok körülbelül 85%), és a választandó gyógyszer. Az ajánlott dózis 750 mg naponta háromszor öt napig (vagy legalább> 3 nap). A gyermekek számára 15 mg/kg/nap, három adagban ajánlott. Egyéb hatásos gyógyszerek közé tartoznak: kvinakrin (Atabrine®), tinidazolt (Fasigyn®), furazolidone (Furoxone®), és paramomycin (Humatin®). Tinidazol hatásos, mint egy két gramm dózis; paramomycin nem szívódik, és hasznos lehet a terhesség alatt.
Széleskörű elterjedése a Giardia és fertőzőképesség a ciszták miatt nem valószínű, hogy az emberi fertőzés teljesen meg fognak szűnni. Ellenőrző intézkedések megelőzése vagy csökkentése Giardia fertőzés függ az adott körülmények között az átviteli, de általában bevonják intézkedéseket, amelyek megakadályozzák a szervezetbe kerülő anyagok szennyezett széklet (lásd széklet-szájon átviteli tényezők). Az egészségfejlesztés és az oktatás javítását célzó személyi higiénia, valamint hangsúlyozva kézmosás, higiénia és élelmiszer-kezelés, hatékony ellenőrzési tevékenység csökkentésére irányuló személy-személy átvitel. Külön figyelmet a személyes higiénia magas kockázatú helyzetekben, mint a napközi és más intézmények szükséges. Kezelése tünetmentes háztartás tagjainak megakadályozza az újrafertőződés nem endémiás területeken. Értéke azonban kezelésére tünetmentes hordozók hiperendémiás közösségek megkérdőjelezhető, mivel az újrafertőződés aránya magas. A társadalmi-gazdasági helyzet számos fejlődő országban megnehezíti a fertőzés megelőzésére. Közegészségügy védelmét célzó intézkedések vízellátó szennyeződés van szükség, hogy megakadályozzák a járványok, és csökkentsék endémiás. A turisták ne igyon csapvizet további kezelés nélkül olyan helyeken, ahol a tisztasági megkérdőjelezhető. Forráspont vagy jód kezelés elpusztítja Giardia ciszták, de normál klórozás nem. Nincsenek biztonságban vagy hatékony chemoprophylatic gyógyszerek Giardiasis.
TRICHOMONIASIS
• Trichomonas Morfológia és fajok
• Váltó és életciklus
• Tünetek és patogenezise
• Diagnózis, kezelés és vezérlés
A trichomonádok egy csoportja ostoros egysejtűek. A legtöbb e csoport tagjai parazita és csak néhány szabadon élő fajt azonosítottak. Általában a trichomonádok nem patogén kommenzális, és csak néhány faj fontos az állatokban és emberekben. Négy faj trichomonádok megfertőzni embereket (táblázat). Ezek közül csak a Trichomonas vaginalis egyértelműen patogén, és ez általában alacsony virulenciájú. A többiek mutatnak megkérdőjelezhető patogenitás.
|
Trichomonádok az emberek |
||||||||||
|
A trichomonádok emberek élnek különböző anatómiai helyeken. T. vaginalis egy gyakori szexuális úton terjedő betegség, amely megtalálható az urogenitalis traktus. T. Tenax, más néven T. buccalis, egy kommenzalista az emberi szájüregben talált főleg olyan betegeknél, rossz szájhigiénia és a fejlett fogágybetegség. T. Tenax, vagy egy szervezet olyan hasonló morfológiájú is esetenként a tüdőben találhatók meg. Ilyen esetekben számoltak főleg olyan betegeknél szolgáló rákos vagy egyéb tüdőbetegségek vagy műtétet követően. Pentatrichomonas hominis, korábbi nevén Trichomonas hominis, egy nem-patogén kommenzalista a vastagbél (lásd nem patogén bél ostoros). Egyes szerzők osztják a trichomonádok három nemzetségek száma alapján a szabad csillóval. Faj három csillóval nevezzük Tritrichomonas, ezek négy nevezik Trichomonas és Pentatrichomonas utal trichomonádok öt szabad anterior csillóval. Dientamoeba fragilis eredetileg úgy vélik, hogy egy ameba (lásd nem patogén bél ameba). Most már tudjuk, hogy egy ostoros-Azonban nélkül flagellumszerű kapcsolódó trichomonádok.
A megkülönböztető jegye a trichomonádok egy axostyle (ax), amely végigfut a szervezet, és úgy tűnik, hogy ne nyúljanak a hátsó vége (ábra). A axostyle egy citoszkeletális elem amely koncentrikus sorok a mikrotubulusok és úgy vélik, hogy működnek a zár a parazita hámsejtek. Trichomonádok is jellemzi 4-6 csillók (fg) kikerülő az elülső végén. Az egyik csillók csatlakozik a test a szervezet és képez utólagosan-irányított hullámzó membrán (um), míg a fennmaradó flagellumok ingyenes. Az egyesített bazális testek (bb), és az alapja a hullámos membrán, úgynevezett Costa (cs), gyakran látni a festett készítmények. Ritkábban látták az cytostomal horony (cy). Egyetlen sejtmagból (nu) található meg az elülső végén a parazita.
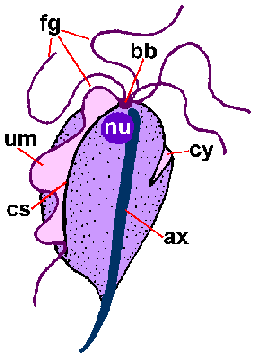
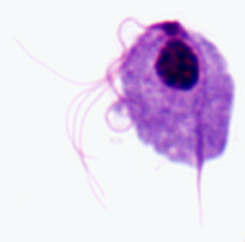
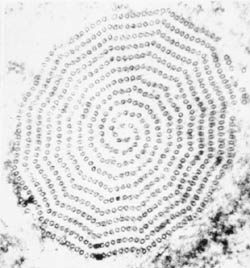
Sematikus ábrázolása jelentős szerkezeti jellemzői trichmonads (balra). Giemsa-festett trophozoite T. vaginalis in vitro kultúrában (középen). Elektronmikroszkópos képe axostyle keresztmetszet mutatja koncentrikus sorai mikrotubulusok (jobbra).
A trichomonádok, mint sok más bélrendszeri egysejtűek mutatnak anaerob anyagcsere és hiányzik a mitokondriumok. Része az energia-anyagcsere trichomonádok magában egyedülálló organelle úgynevezett hidrogenoszóma. A hidrogenoszóma kettős membrán és távoli rokonságban a mitokondrium. Azonban hiányzik belőle a DNS, citokrómok és számos tipikus mitochnondrial funkciók, mint az enzimek, a trikarbonsav ciklus és az oxidatív foszforiláció. Az elsődleges funkciója a hidrogenoszóma az anyagcserét a piruvát, során termelt glikolízis belül a citoszolban, hogy acetát és szén-dioxid egyidejű ATP termelésben. Az elektronok kiadás az oxidációs piruvát át hidrogén ionok előállítására molekuláris hidrogén, innen a név hidrogenoszóma.
TRICHOMONAS VAGINALIS
Trichomonas vaginalis írták le először származó gennyes hüvelyi bevezetések 1836 és az elején a huszadik század elismert, mint etiológiai ágens hüvelygyulladás. Trichomoniázis gyakori szexuális úton terjedő betegség az egész világon elterjedt és a becslések szerint 167 millió ember megfertőződnek évente világszerte és 5 millió új fertőzést évente az Egyesült Államokban. Trichomoniázis úgy vélik, hogy a leggyakoribb nem-vírus szexuális úton terjedő betegség. Annak ellenére, hogy a gyakorisága trichomoniázis azt a múltban tartották inkább kellemetlen parazita helyett egy jelentős kórokozó. Azonban ma már egy tényező előmozdításában HIV-fertőzés (lásd a keretben), ami az alacsony súly és a koraszülés, és hajlamosít a nők jelentős kényelmetlenség és a stressz.
|
Trichomonas és HIV |
A patológia által okozott Trichomonas fokozhatják hatékonyságát a HIV-átvitel (1). T. vaginalis fertőzés jellemzően vált ki helyi sejtes immunválasz gyulladás a hüvelyi hámszövet és méhnyak nőknél és a húgycső a férfiak. Ez a gyulladásos válaszreakció magában foglalja a beszivárgása potenciális HIV-célsejtek, mint például a CD4 + hordozó limfociták és a makrofágok. Ezen túlmenően, a T. vaginalis punctata vérzések a hüvely falát és a méhnyak. Ez a leukocita infiltráció és a genitális léziók számának növelése a célsejtek a vírus számára, és lehetővé teszi a közvetlen vírus-hozzáférést biztosít a véráramba keresztül nyitott elváltozások. Ezen túlmenően, a vérzések és gyulladás szintjének növelése vírus testnedvekben, és a számok a HIV-fertőzött limfociták és makrofágok jelen a genitális területen személyek már HIV-vel fertőzött. Ez a növekedés a szabad vírus és vírusfertőzött leukociták növelheti annak valószínűségét, HIV expozíció és továbbítása egy nem fertőzött partner. Fokozott nyaki ontásán HIV kimutatták, hogy társítható nyaki gyulladás, és jelentősen növelte a vírusterhelést sperma dokumentálták férfiak trichomoniasis. Továbbá, mivel sok beteg Trichomonas fertőzés tünetmentes, vagy csak enyhe tüneteket okoz, akkor valószínű, hogy maradnak szexuálisan aktív ellenére fertőzés.
|
T. vaginalis, a neve ellenére fertőzi férfiak és nők egyaránt. Nőkben a szervezet elsősorban él a hüvely, és férfiakban ez általában megtalálható a húgycső, a prosztata vagy mellékhere. Az életciklus az csak egy trophozoite szakaszban továbbított közvetlen érintkezés közösülés során. Nem nemi átvitel ritka, de lehetséges, mert a trophozoiták képes túlélni 1-2 nap vizeletben és 2-3 órán át egy nedves szivaccsal. Ezen túlmenően, neonatals már fertőzött során a szülés folyamán. A trophozoiták élő szorosan kapcsolódó vagy csatlakozik a hám az urogenitális traktus, ahol lemásolni bináris hasadási.
TÜNETEK ÉS PATOGENEZISE
|
Klinikai megjelenési formái |
|
|
A nőstények |
A hímek |
|
|
| *% a fertőzött; **% a tüneti | |
T. vaginalis okozza különböző klinikai megnyilvánulásai a férfiak és a nők és a nők (táblázat), nagyobb valószínűséggel mutatnak tüneteket, amelyek hajlamosak hosszabb ideig fennállhat. Az inkubációs időszak jellemzően tól 4-28 nap. Nőkben a fertőzés tud mutatni, mint egy enyhe hüvelygyulladás, egy akut vagy krónikus vulvovaginitis, vagy urethritis. A jelentkező vagy súlyosbodó tünetek gyakran fordul elő, vagy közvetlenül utána menstration. A leggyakoribb panasz kapcsolódó T. vaginalis fertőzés tartósan enyhe hüvelygyulladás társított bőséges, kellemetlen szagú folyás, amely gyakran kíséri égő vagy viszkető. Ez kisülés leggyakrabban szürke, de lehet sárga vagy zöld, és időnként habos vagy vérrel színezett. A mentesítés csökken, mint a fertőzés egyre krónikus. Sok nő tapasztal fájdalmas vagy nehéz közösülés. Húgycső részvétel előfordul számos esetben és jellemzi a vizelési zavar (fájdalmas vizelés), és gyakori vizelés.
A vaginális hámszövet az elsődleges fertőzés helyén. Így a hüvelyi falak általában erythemás (azaz piros) és mutathat kiütéses (a kis nem-emelt spot) vérzések. Punctata vérzések a méhnyak, az úgynevezett eper méhnyak, figyelhetők meg körülbelül 2% -ában. Ez eper méhnyak egy jellegzetes patológiai megfigyelés kapcsolódó trichomoniasist nem látott más szexuális úton terjedő betegségek.
A hímek valószínűleg tünetmentes (50-90%), és a fertőzés általában a önkorlátozó. A húgycső és a prosztata a leggyakoribb helyei fertőzés. Gyakori tünetek: húgycső kisülés (kezdve kevés a gennyes), vizelési és húgycső pruritus (viszketés). Néhány férfi tapasztal égő után azonnal közösülést.
Keveset tudunk a patofiziológia társított T. vaginalis fertőzés, de feltehetően közötti kölcsönhatásokat a parazita és a fogadó hámsejtek. In vitro vizsgálatok azt mutatják, hogy a T. vaginalis képes elpusztítani a sejteket egy kapcsolattartó függő módon. Ezért tapadást a trophozoiták a hám úgy vélik, hogy egy jelentős tényező a patogenezisében. Számos adhéziós fehérjét azonosítottak a felszínen a trophozoiták. Ezen túlmenően, szekretált proteázok, amelyek szerepet játszanak a patogenezisében is fény derült.
DIAGNÓZIS, KEZELÉS ÉS ELLENŐRZÉS
Általában a klinikai tünetek nem megbízhatóak, mint egyetlen eszköz a diagnózis, mivel a klinikai prezentáció hasonló más STD-k, és sok beteg enyhe, vagy nincsenek tünetei. Diagnózist demonstrációja trophozoiták vaginális, húgycső, prosztata váladék, vagy a vizelet üledékben (következő prosztata masszázs). Mikroszkópos vizsgálata nedves tartók friss hüvelyváladék, lehetőleg gyűjtött egy speculum egy vattapálcikával, a legpraktikusabb módja a diagnózis. A mintákat hígítani kell sóoldattal, és megvizsgálta azonnal. T. vaginalis által elismert jellegzetes morfológiai jellemzői (lásd fent), és annak gyors szaggatott mozgékonyságát. Példányok is fixáljuk és Giemsa vagy fluoreszcens festékkel. Azonban a szervezet nehéz lehet felismerni a festett metszeteken.
Az érzékenység közvetlen megfigyelés tól 40-80%. Ezért az in vitro kultúra tartják a diagnosztikai etalonnak ellenére bizonyos korlátai. Például az eszközökhöz való szükséges és szervezetekre van szükség 2-7 napos tenyésztés előtt azokat felismerik. A hozzáférhetőség kérdése részben megoldódott a InPouch™ TV tenyésztési rendszer (Biomed Diagnostics). Ez egy kereskedelmi forgalomban kapható önálló rendszer kimutatására T. vaginalis klinikai mintákban. Az antitest és a DNS-alapú vizsgálatok nagy érzékenysége és specificitása fejlesztenek.
Metronidazol (Flagyl®), és más nitroimidazolok, mint például a tinidazol, amelyek igen hatásos trichomoniasis. A metronidazol aktiválódik a hydrogensome egy nitrocsoport ion közbenső terméket kapunk. Alkalmazhatunk egyetlen két gramm adag (85-92% -os gyógyulási arány), illetve 250 mg-os három alkalommal naponta 7-10 napig (> 95% -os gyógyulási arány) lehet használni. Szexuális partner kell kezelni egyidejűleg, hogy megakadályozzuk. Néhány gyógyszer-rezisztencia leírták, de ez nem egy elterjedt probléma. Kezelési hibák általában miatt be nem vagy fertőzések ellen.
Epidemiológiája trichomoniasist kiállítási funkciók hasonló más szexuális úton terjedő betegségek (doboz)
|
Trichomoniázis mint STD |
|
és előfordulási korrelál a szexuális partnerek száma. Ezen túlmenően, társfertőzés más STD-k gyakori. Úgy becsülik, hogy akár 25% -a szexuálisan aktív nők megfertőződhetnek egy bizonyos ponton az életük során, és a betegség továbbítják 30-70% -a férfi partnerek. Alkalmazott intézkedések a kontroll a többi STD, mint például a korlátozó szexuális partnerek száma és az óvszer használata, szintén hatékony megelőzése trichomoniasis.
Vélemények az Trichomoniázis:
- Lehker, M.W. and Alderete, J.F. (2000) Biology of trichomonosis. Current Opinion in Infectious Diseases 13, 37-45.
- Petrin, D., Delgaty, K., Bhatt, R., Garber, G. (1998) Clinical and microbiological aspects of Trichomonas vaginalis. Clin. Microbiol. Rev. 11: 300-317.
- Schwebke, J.R. and Burgess, D. (2004) Trichomoniasis. Clinical Microbiology Reviews 17, 794-803.
DIENTAMOEBA FRAGILIS
Dientamoeba fragilis eredetileg le, mint egy ameba alapján morfológiája. Azonban később felismerték, hogy mutat egy morfológiája jobban hasonlít a pulyka parazita Histomas meleagridis, kivéve a hiányzó mozgásképességet. Ultrastruktúrális tanulmányok rámutatnak, a hasonlóság az trichomonádok, beleértve a birtokában hidrogenoszóma és molekuláris vizsgálatok megerősítették szoros filogenetikai kapcsolata Dientamoeba és Histomas és egy esetleges távolabbi kapcsolatban Trichomonas.
Mint más trichomonádok, Dientamoeba csak mutat trophozoite szakaszban (ábra). Ez felvet néhány kérdést a átviteli mód, hogy egy ciszta a szakaszban általában részt vesz a széklet szájhagyomány. Ezen túlmenően, a trophozoiták a Dientamoeba túlélni a testen kívül egy nagyon rövid idő alatt. H. meleagridis is hiányzik a ciszta szakaszban, és kimutatták, hogy keresztül kell továbbítani, a tojásokat egy fonalféreg. Mivel a szoros kapcsolatát Histomas és Dientamoeba, azt javasolják, hogy Dientamoeba is keresztül továbbított bélféreg tojás. Epidemiológiai és kísérleti bizonyítékok a bűncselekménnyé a pinworm Enterobins vermicularis hordozóként a Dientamoeba. Újabban, sertés kimutatták, hogy egy természetes gazda számára D. fragilis azonos genotípusú talált emberekben, így növelve a lehetőséget a zoonózis átviteli (Cacciò et al, Emerg Infect Dis 18(5):838–841, 2012).
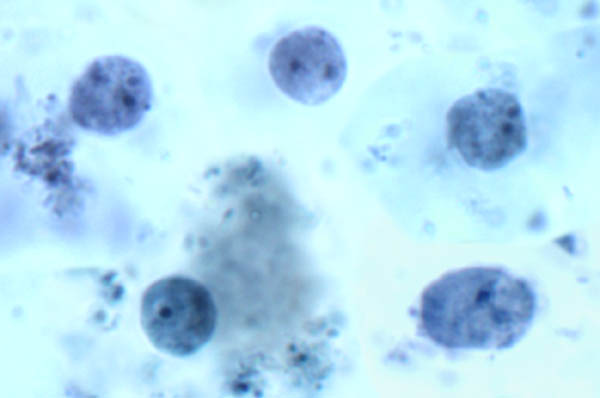
Morfológiája Dientamoeba fragilis egy székletminta. Trophozoiták mutatnak ameba morfológia és gyakran bi-nukleált.
Történelmileg Dientamoeba tartották, mint egy nem-patogén kommenzalista. Azonban a klinikai tünetek gyakran korrelál a jelenléte nagyszámú trophozoiták és a kezelés a fertőzés megoldja a tüneteket. A tünetek előfordulási gyakorisága a becslések szerint 15-30% -a fertőzött egyének. Klinikai tünetek kapcsolódó Dientamoeba közé szakaszos hasmenés, hasi fájdalom, puffadás, émelygés és fáradtság. Keveset tudunk a patogenezis és Dientamoeba valószínűleg működik, mint egy alacsony minőségű irritáló bél nyálkahártya-felületek, amelyek vezethet, hogy bizonyos gyulladást. Iodoquinol általában a választandó szer kezelésére Dientamoeba. Paromomycin és metronidazol is hatékony.
Vélemények az Dientamoeba
- Johnson et al (2004) Emerging from obscurity: biological, clinical, and diagnostic aspects of Dientamoeba fragilis. Clin Microbiol Rev 17:553.
- Barratt JL et al (2011) A review of Dientamoeba fragilis carriage in humans: several reasons why this organism should be considered in the diagnosis of gastrointestinal illness. Gut Microbes 2:3–12.
BALANTIDOSIS
Balantidium coli a csak csillós amely embereket fertőz. Megállapítást nyer világszerte, de mint sok más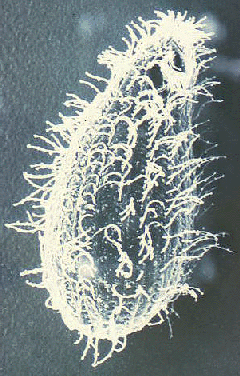 széklet-szájon úton terjedő betegségek, sokkal gyakoribbak a trópusokon. Azonban az előfordulási arányok ritkán haladja meg az 1%. B. coli is fertőz sokféle emlősök és különösen gyakori a majmok és sertés. Előfordulása a sertések között mozog 20-100% és az emberi balantidiosis általában mutat fokozott előfordulási közösségekben élnek szoros együttműködésben disznók. Például Pápua Új-Guinea, ahol sertéseket a fő háziállatok, a előfordulás sertés pásztorok és vágóhídi dolgozók számoltak be, hogy olyan magas, mint 28%. Emberről emberre terjedő fertőzés is dokumentálták, és ez az átviteli mód is valószínű olyan környezetben, ahol a zsúfoltság és a rossz személyi higiéniai, mint a mentális és börtönök. (Skip általános csillós biológia)
széklet-szájon úton terjedő betegségek, sokkal gyakoribbak a trópusokon. Azonban az előfordulási arányok ritkán haladja meg az 1%. B. coli is fertőz sokféle emlősök és különösen gyakori a majmok és sertés. Előfordulása a sertések között mozog 20-100% és az emberi balantidiosis általában mutat fokozott előfordulási közösségekben élnek szoros együttműködésben disznók. Például Pápua Új-Guinea, ahol sertéseket a fő háziállatok, a előfordulás sertés pásztorok és vágóhídi dolgozók számoltak be, hogy olyan magas, mint 28%. Emberről emberre terjedő fertőzés is dokumentálták, és ez az átviteli mód is valószínű olyan környezetben, ahol a zsúfoltság és a rossz személyi higiéniai, mint a mentális és börtönök. (Skip általános csillós biológia)
ÁLTALÁNOS CSILLÓS BIOLÓGIA
Csillósok egy nagy és változatos csoportja egysejtűek. A legtöbb csillósok szabadon élő és megtalálhatók a különböző élőhelyeket. Jól ismert csillósok közé Paramecium faj, amely megtalálható a tavak az egész világon, és Ichthyophthirius multifiliis, külső élősködők hal okozza a fehér folt betegség (más néven “ick). Ahogy a neve is mutatja, csillósok rendelkeznek csillók valamikor élete során ciklusokat. A csillók általában elrendezve hosszanti sorokban, és jellemzően fedik a felületet a szervezet. Csillósok is jellemzi nukleáris dimorfizmus éltek, hogy két különálló magok. A nagy vese alakú macronucleus részt vesz a “housekeeping” vagy szomatikus funkciók a sejt, míg a kisebb gömbalakú mikronukleusz tartalmazza a teljes genomban. A macronucleus tartalmaz több ezer példányban transzkripció szempontjából aktiv “minikromoszómák” képviselő 10-20.000 különböző DNS-molekulákat. Ez számos telomerek (kromoszóma végek) eredményezett csillósok hogy egy korai modell rendszer a tanulmány a telomerek és a telomeráz (az enzim, amely szintetizálja a telomerek).
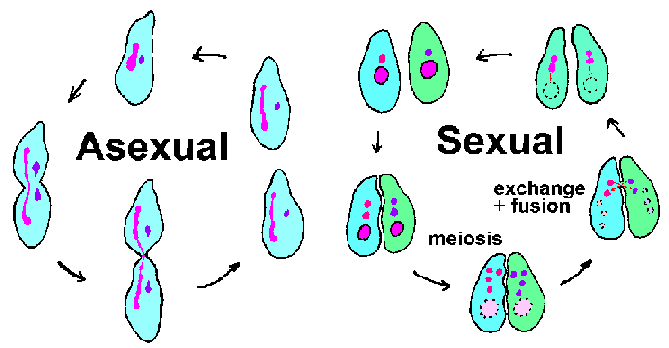
Csillósok mennek mind az ivartalan szaporodás (azaz bináris hasadási) és ivartalan szaporodás bevonásával konjugáció (ábra fent). Konjugáció során, két csillósok az ellentétes párosodási típusú párt és a génállomány. A házastársi érintkezés váltja ki a meiózis a mikronukleuszban eredményeként 4 haploid mikronukleuszban. Egyidejűleg a macronucleus elromlik, és eltűnik. Három mikronukleuszban szétesik, és a fennmaradó mikronucleus osztja újra. Mind a konjugáló szervezetek adományoz egy mikronukleusz (ivarsejt vagy férfi), hogy a párja keresztül citoplazma híd, ami összeköti őket. Az ivarsejt mikrosejtmag egybeolvad az álló (vagy nő) mikrosejtmag képező diploid zigóta mikronucleus. A conjucating pár válik, és a zigóta nucluei mennek újabb részlege. Az egyik ilyen mikronukleuszok alakul a az macronucleus, így teljessé a ciklust. Kialakulása az macronucleus magában töredezettsége a kromoszómák és a veszteség a megfelelő DNS-szekvenciák a gének nem magas szinten expresszálódnak a normális ivartalan ciklus. A maradék DNS-fragmentumok, vagy minikromoszómák, majd amplifikáltuk. (Lásd az ábrát DNS feldolgozás során macronucleus kialakulását.)
BALANTIDOSIS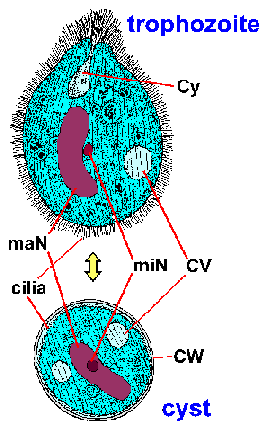
B. coli általában él, mint egy nem-patogén commensalis a vastagbélben, és nem okoz tüneteket. Felületes gyulladás a vastagbél-nyálkahártya kerülhet sor, amely azt eredményezheti, hasmenés és kólikás fájdalom. Enyhe vagy krónikus fertőzések jellemzi szakaszos hasmenés és székrekedés, fogyás, és a hasi fájdalom. Ritka esetekben a trophozoiták megtámadják a bél nyálkahártya és termel fekély. Klinikailag ez azt eredményezi, egy akut hasmenés nyálka és a vér (azaz, vérhas). Ez balantidial vérhas hasonló a vérhas által termelt Entameoba histolytica (lásd alább). Ritka extraintestinalis fertőzések bevonásával tüdő, vagina, ureter és a húgyhólyag és a bél perforáció vezető hashártyagyulladás számoltak be.
Laboratóriumi diagnózis azonosításával a szervezet a székletben. Balantidium mutat egy tipikus széklet-szájon életciklusa álló trophozoite és ciszta szakaszaiban. A nagy méretű, egyedi morfológiai jellemzőit Balantidium (ábra) kizárja a összetéveszthető bármilyen más egysejtűek megtalálható az emberi ürülék. A trophozoite van tojásdad és átlagos mérete 70 x 45 um, de terjedhet felfelé 150-200 Lm. A ciszta van egy jellegzetes ciszta fala (CW), és több, gömb alakú, amelynek átlagos átmérője 55 Lm. Ebben festett példányok a legnyilvánvalóbb belső szerkezete a nagy macronucleus (maN). A mikronukleusz (miN) nem mindig nyilvánvaló, mert a szoros együttműködésben a macronucleus. Összehúzó vacuoles (CV), amely funkció ozmotikus szabályozás, gyakran látható, esetenként a cytostome (Cy) kimutatható. Hasonlóan más csillósok, Balantidium borítja sorai csillók. A csillók ad a parazita felszínén fuzzy megjelenést, és kevésbé hangsúlyos a ciszta szakaszban.
A kezelés a választás tetraciklin megadott négyszer 500 mg naponta, 10 napig. Iodoquinol az ajánlott alternatív gyógyszer. Metronidazol nem termelt következetes eredményt. Megelőző intézkedések megegyeznek a más betegségek által továbbított széklet-szájon (lásd széklet-orális átvitel faktorok vagy vita Giardia megelőzés). Ezen kívül, a sertés csatornázás kell tartani távol ellátás ivóvíz és élelmiszer.
AMEBIASIS
Több tagja a nemzetség Entamoeba megfertőzni embereket (lásd alább). Ezek közül csak az E. histolytica tartják kórokozó a betegséget okoz az úgynevezett amebiasis vagy amebic vérhas. E. dispar morfológiailag azonos az E. histolytica, és a két korábban úgy, hogy az azonos faj. Azonban, genetikai és biokémiai adatok jelzik, hogy a nem-patogén E. histolytica egy elkülönült fajra (lásd tárgyalását kritériumok). A két faj található az egész világon, de mint sok más bélrendszeri protozoon, sokkal gyakoribbak a trópusi országokban vagy más területeken gyenge higiénés körülmények. Úgy becsülik, hogy legfeljebb 10% -át a világ népességének lehet fertőzött vagy E. histolytica vagy E. dispar és sok trópusi országban az előfordulási közelítheti 50%. Vannak a becslések szerint 50 millió esetben amebiasis évente akár 100.000 halálesetet.
• Életciklus és morfológia
• Patogenezise
• Lehetséges mechanizmusok patogenezise
· Sematikus ábra az Trophozoite invázió
• Klinikai előadás
• Diagnózis, kezelés és vezérlés
ÉLETCIKLUS ÉS MORFOLÓGIA
E. histolytica mutat egy tipikus fekális-orális életciklusa álló fertőző ciszták telt el a széklet és a trophozoiták amely replikálódnak a vastagbélben. A fertőzés során szerzett elfogyasztását ciszták és a kockázati tényezők hasonlóak más betegségek által továbbított széklet-szájon (lásd a táblázatot). Szennyezett élelmiszer és a víz valószínűleg az elsődleges forrásai a fertőzés. A magasabb előfordulási területeken alacsonyabb társadalmi-gazdasági státusz valószínűleg a rossz higiéniai körülmények és a hiányzó vízvezeték. Azonban E. histolytica ritkán az oka utazók hasmenése, és rendszerint együtt jár a hosszú távú (> 1 hónap) marad endémiás területre. A nagyobb arányú E. histolytica fertőzés is megfigyelhető intézmények, mint a pszichiátriai kórházakban, árvaházakban és börtönökben, ahol zsúfoltság és a problémák széklet szennyeződés kiváltó tényezők. A magas előfordulás homoszexuálisok is megfigyelték. Az ember az egyetlen gazda E. histolytica és nincsenek állatok tározók.
Esetén lenyelés a ciszták áthaladnak a gyomor és excyst az alsó része a vékonybélben. Excystation jár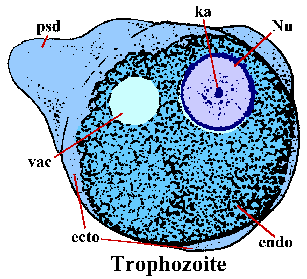 zavar a ciszta fala és a quadranucleated ameba derül ki a nyíláson. A ameba megy egy újabb nukleáris részlege, majd három egymást követő fordulóban citokinezist (azaz sejtosztódás), hogy nyolc kis uninucleated trophozoiták, néha amebulae. Ezek az éretlen trophozoiták megtelepedni a vastagbél, főleg a vakbélben és sigmoidorectal régiókban, ahol táplálkoznak baktériumokat és sejttörmeléket és mennek keresztül ismételt fordulóban bináris hasadási.
zavar a ciszta fala és a quadranucleated ameba derül ki a nyíláson. A ameba megy egy újabb nukleáris részlege, majd három egymást követő fordulóban citokinezist (azaz sejtosztódás), hogy nyolc kis uninucleated trophozoiták, néha amebulae. Ezek az éretlen trophozoiták megtelepedni a vastagbél, főleg a vakbélben és sigmoidorectal régiókban, ahol táplálkoznak baktériumokat és sejttörmeléket és mennek keresztül ismételt fordulóban bináris hasadási.
E. histolytica trophozoiták van egy amorf forma és általában 15-30 jim átmérőjű. A trophozoiták mozognak kiterjesztésével egy ujjszerű pseudopodium (psd) és húzza a többi test előre (úgynevezett ameboid mozgás). Állábai, és néha a külső széle a trophozoite, egyértelmű fénytörő megjelenését, és a továbbiakban az ektoplazma (ecto). A többi a citoplazma egy szemcsés megjelenésű és az úgynevezett endoplasm (endo). Alkalmanként a glikogén vacuole (vac) nyilvánvaló. Nukleáris (Nu) morfológia foltos példányok jellemzi finoman szemcsés gyűrű perifériás kromatin és egy központosán elhelyezett karyosome (ka).
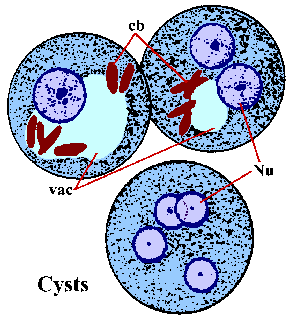 Alternatívájaként aszexuális replikációs trophozoiták is encyst. A felelős tényezők indukciójában encystation nem ismertek. Encystation kezdődik a trophozoiták egyre gömb alakú, és a megjelenése chromatoid szervek a citoplazmában. Chromatoid szervek (cb) festjük hosszúkás szerkezetek körnek vége és képviseli a összesítése riboszómák. A ciszta fala áll kitin és sima fénytörő megjelenést. Ciszta érés során két fordulóban a nukleáris replikáció nélkül sejtosztódás és ciszták 1-4 magok (Nu) megtalálható a székletben. A nukleáris morfológiája a ciszta hasonló a a trophozoite kivéve, hogy a sejtmagok válik egyre kisebb követő részlege. Előfordul, hogy a fiatal ciszták (azaz 1-2 atommag) lesz glikogén vacuole (vac) fog megjelenni, mint egy tiszta területet festett példányok. Ez vacuole néha kiszorítja, és megváltoztathatja a morfológia a magok. A chromatoid szervek eltűnni látszanak, mint a ciszta megérik. A ciszták általában 12-15 lm átmérőjű. Ciszták azonnal fertőző után ürül a széklettel és életképes lesz hetekig-to-hónapra környezeti feltételektől függően.
Alternatívájaként aszexuális replikációs trophozoiták is encyst. A felelős tényezők indukciójában encystation nem ismertek. Encystation kezdődik a trophozoiták egyre gömb alakú, és a megjelenése chromatoid szervek a citoplazmában. Chromatoid szervek (cb) festjük hosszúkás szerkezetek körnek vége és képviseli a összesítése riboszómák. A ciszta fala áll kitin és sima fénytörő megjelenést. Ciszta érés során két fordulóban a nukleáris replikáció nélkül sejtosztódás és ciszták 1-4 magok (Nu) megtalálható a székletben. A nukleáris morfológiája a ciszta hasonló a a trophozoite kivéve, hogy a sejtmagok válik egyre kisebb követő részlege. Előfordul, hogy a fiatal ciszták (azaz 1-2 atommag) lesz glikogén vacuole (vac) fog megjelenni, mint egy tiszta területet festett példányok. Ez vacuole néha kiszorítja, és megváltoztathatja a morfológia a magok. A chromatoid szervek eltűnni látszanak, mint a ciszta megérik. A ciszták általában 12-15 lm átmérőjű. Ciszták azonnal fertőző után ürül a széklettel és életképes lesz hetekig-to-hónapra környezeti feltételektől függően.
PATOGENEZISE
E. histolytica gyakran él a commensalis a vastagbél nélkül nyilvánvaló klinikai megnyilvánulásai.
|
Amebiasis haladás |
nem-invazív
invazív
|
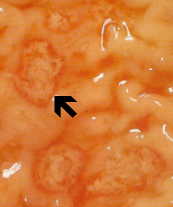
Azonban trophozoiták támadják a vastagbél nyálkahártya és termel fekélyek és vérhas (lásd a keretben). Ez az invazív betegség fokozatosan egyre rosszabb, és vezethet egy komolyabb betegség. A amebas is áttétet más szervekre és termel anextraintestinal amebiasis. Más szóval, az E. histolytica egy fakultatív patogén hogy mutat sokféle virulencia.
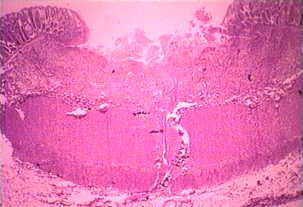
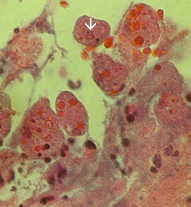
A nem-invazív betegség gyakran tünetmentes, de okozhat hasmenést vagy más gyomor-bélrendszeri tünetek, mint például a hasi fájdalom vagy görcsök. Ez a nem-invazív fertőzés is fennállhat vagy haladást invazív betegség, amelyben trophozoiták behatolnak a bél nyálkahártyáján, és öld meg a hámsejtek. A korai sérülés egy kis terület elhalás vagy fekélyt jellemzi megemelt szélű, és gyakorlatilag nincs gyulladás között elváltozások (ábra). A ameba fog terjedni oldalirányban és lefelé a nyálkahártya alatti (alatta a hám), és megölik gazdasejt ahogy haladnak. Ez azt eredményezi, a klasszikus “lombik alakú” fekély egy kis nyílás és a széles bázis. Trophozoiták vannak többségben határán közötti egészséges szövetet, és a nekrotikus szövet. Ezek invazív ameba vannak elfogyasztásának gazdasejt és trophozoiták az elfogyasztott vörösvértestek sokszor nyilvánvaló. Ezek hematophagous trophozoiták is megtalálhatók a vérhasi széklet. Ciszta gyártás során csökken invazív szakaszában a fertőzés és a ciszták nem található a szöveti károsodást.
Balra: Az üregi oldalán vastagbél származó fulmináns amebiasis esetben mutató több fekély. Megjegyzés megemelt peremmel (nyíl). Középen: szövettani készítménnyel, amely keresztmetszetének fekély. Megjegyzés: a magas fokú elhalás központjában fekély. A amebas haladnak oldalirányban alatt ép nyálkahártya, ahogy azt a microvilli. Jobbra: Nagyobb nagyítással fekély mutató több hematophagous trophozoiták. Az atommag (nyíl) nyilvánvaló egyik amebas. Képek Peters és Gilles (1989), A színes Atlas of Tropical Medicine és parazitológiai (3. kiadás).
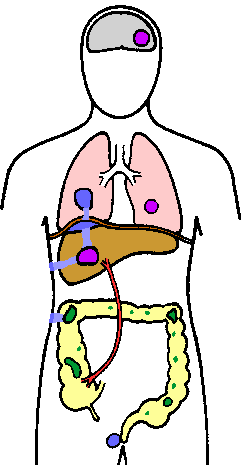
E. histolytica található elsősorban a vastagbélben, ahol meg lehet élni, mint egy nem patogén commensalis vagy megtámadják a bél nyálkahártyáját (zöld). A ameba is áttétet más szervekre keresztül hematogén úton (lila); amely elsődlegesen a portális véna és a máj. A ameba is terjed keresztül direkt expanziós (kék) okozva tüdő fertőzés, bőrelváltozások vagy a végbélnyílás fekélyek.
A fekélyes folyamat továbbra is bővíteni oldalirányban és lefelé. Ha nagyszámú fekélyek vannak jelen, akkor összeolvadnak, amely vezethet lokalizált sloughing le a bélfal. Fekély expanzió is behatolnak a savós réteg és vezet a perforáció a bélfalon. Ez a perforáció vezethet helyi tályogok vagy generalizált hashártyagyulladás. (Lásd még a vázlatos ábrázolása szöveti invázió.) Amebic fekélyek is válhat másodlagosan fertőzött baktériumok megzavarhatja a klinikai képet. Ezen túlmenően, az E. histolytica fertőzés esetenként képződéséhez vezet egy amebic granuloma, más néven ameboma. A ameboma gyulladásos megvastagodása a bélfalon körül a fekélyt, amely lehet összetéveszteni a tumor.
Amebiasis is elért egy szisztémás, vagy extraintesztinális fertőzés. Terjesztése az elsődleges bél lézió túlnyomórészt keresztül a véráramba, de ugyancsak előfordulhat a közvetlen meghosszabbítása az elváltozás. A máj a leggyakrabban érintett szerv, és ez valószínűleg a közvetlen szállítását trophozoiták a vastagbélben a májba májkapugyűjtőér (ábra). Kezdetben az elváltozások kis gócok nekrózis, amely gyakran összefonódik egyetlen tályog, mert bővíteni. Ez a máj tályog továbbra is a képre a trophozoiták fokozatosan elpusztítja, és ne nyelje gazdasejt. A központ a tályog, amely a lizált májsejtek vörösvértestek, epe és kövér, lehet cseppfolyóssá ez elhalt anyag (néha helytelenül nevezik genny) lesz a színe a sárgás-vörösesbarna. Másodlagos bakteriális fertőzések a máj tályog nem gyakori (~ 2%).
Hematogén terjedése trophozoiták más oldalakra, például a tüdő vagy az agy, ritka, de előfordul. A második leggyakoribb extraintesztinális site után a máj a tüdőbe. Légúti fertőzések általában származhat közvetlen kiterjesztése a máj elváltozás a membránon keresztül, és a mellhártya és a tüdő. Bőrelváltozások eredményeként jött létre a máj – vagy bél sipoly is előfordulhat, bár rendkívül ritka. Más bőrelváltozások közé perianális fekély és bevonása a nemi szervek, beleértve a pénisz homoszexuálisok. Ezek a későbbi megnyilvánulásai valószínű oka, hogy a bőr vagy a nyálkahártyák érintkező invazív trophozoiták.
LEHETSÉGES MECHANIZMUSOK PATOGENEZISE
Amint a fentiekben tárgyaltuk, az E. histolytica kórokozó hogy mutat széles spektrumát virulencia,
|
Entamoeba prevalencia |
|
kezdve egy avirulens kommenzalista a rendkívül invazív és pusztító organizmus (lásd a tárgyalást a patogenitás vs. virulencia). Néhány ilyen különbség a virulencia magyarázható, hogy létezik a morfológiailag azonos, de avirulens, E. dispar. E. dispar soha nem társult tünetekkel invazív betegség és fertőzés nem váltanak szérum antitesteket. Ezzel szemben, az anti-ameba humorális választ figyeltek meg mind a tünetmentes és tünetekkel járó E. histolytica fertőzés. Ez arra utal, hogy még a tünetmentes esetben van egy korlátozott mennyiségű invázió. Azonban fertőzés E. histolytica nem mindig vezet invazív betegség, bár az, hogy csak mintegy 10% -a fertőzött egyének fog kidolgozni tüneti invazív amebiasis. A felelős tényezők patogenezisében E. histolytica nem ismertek. Az egyik megközelítés, hogy megértsék a patogenezise összehasonlítani lehetséges virulencia faktorok között a két közeli rokon.
házigazda tényezők
parazita tényezők
|
Patológiai eredmények gazda-parazita kölcsönhatások, és ezért, a fogadó tényezők, parazita faktorok vagy a kettő kombinációja hozzájárulhat a betegség. Például a fejlesztési invazív betegség oka lehet a mennyiségi vagy minőségi szempontból a gazda immunválasz. Neutrofil sejtek toborzása és intenzív gyulladása figyelhető meg a korai szakaszában amebic invázió. Azonban, gyulladás környező létrehozott fekélyeket és tályogok, ha gyakran minimális szintje miatt szöveti károsodás.
A természet a védő immunválaszok nem világos. Veleszületett vagy nem specifikus immunitás, valamint a szerzett immunitás, valószínűleg mind fontos a megelőzés az invazív betegség. A nyálkahártya-réteg, amely a epitheilial sejtek közötti érintkezés megakadályozásához trophozoite és a befogadó sejteket. Ezen túlmenően, nyálkahártya-IgA válaszok nem fordulhat elő, ha a fertőzés és széklet IgA-ellen trophozoite felületi lektin (lásd Eh-lektin) vannak társítva egy kisebb előfordulási gyakoriságát új E. histolytica fertőzések. Magas titerű szérum antitestek is kialakulhat májbetegségben tályogok. Azonban, mivel a invazív betegség gyakran progresszív és szüntelen, a szerepe ezeknek az anti-ameba antitestek kérdéses. Sejtközvetített válaszok tűnik, hogy szerepet játszanak mértékének korlátozására invazív amebiasis és védi a gazdaszervezetet a kiújulás következő sikeres kezelést.
Ellenállás a gazda immunválasz másik lehetséges virulencia faktor, amelyek hozzájárulhatnak a kialakulásához és súlyosbodásához invazív betegség. Például, az egyik fenotípusos különbség E. dispar és E. histolytica az ellenállása az utóbbi komplement által közvetített lízist (lásd E. dispar). Ezen túlmenően, az E. histolytica gyorsan lebomlik szekretoros IgA és esetleg elnyomja a T-sejt-válaszok az E. histolytica antigéneket. E. histolytica is képes sejtek elpusztítására, beleértve a neutrofil és egyéb immun effektor sejtek, egy érintkezés-függő módon. Lysis a neutrofilek is mérgező termékeket, amelyek hozzájárulnak a pusztulását fogadó szövet. Azonban a szerepe a különböző jelenségek patogenezisében nem ismert.
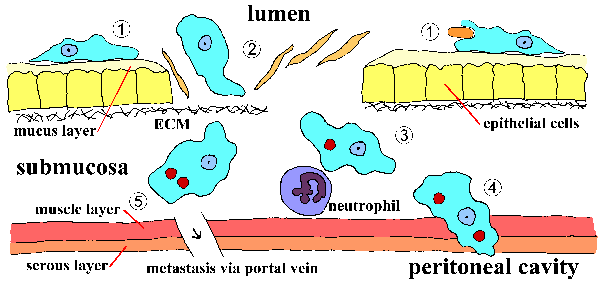
Invázió a bélnyálkahártyán E. histolytica egy aktív folyamat által közvetített parazita és különböző lépéseket lehet ismerni (ábra, kattintson ide a nagyobb kép és részletes legenda). Trophozoiták tartsák be a nyálka réteg (1. lépés). Ez a tapadás önmagában valószínűleg nem járul hozzá a patogenezis és egyszerűen egy mechanizmus a ameba mászni mentén a szubsztrátumhoz. Kimerülése a nyálka barrier lehetővé teszi a trophozoite hogy érintkezésbe hámsejtek. Hámsejtek elpusztulnak egy kapcsolati függő módon, ami zavar a bélnyálkahártya (2. lépés). A trophozoiták továbbra is megöli gazda sejtek a submucosa és tovább megzavarják a szövet, mert előre (3. lépés). Megzavarják a bélfal (4. lépés), vagy metasztázis keresztül a keringési rendszer (5. lépés) is lehetséges. Ragaszkodás, tesztjének és zavar a szövetek fontos tényezői patogenezisében E. histolytica. Parasite fehérjék, amelyek szerepet játszhatnak szerepet ezekben a folyamatokban a következők: Az Eh-lektin, amebapórus, és proteázok.
Eh-lektin. E. histolytica lehet ölni sejtek percen belül tapadt őket az extracelluláris kalcium. Tapadását E. histolytica trophozoiták fogadó sejtek és vastagbél mucinok közvetítik a lektin-aktivitás expresszálódik ameba felszínén. Ez a lektin kötődik galaktóz vagy N-acetil-D-galaktózamin (GalNAc) nagy affinitással és is nevezik galaktóz-gátolható ragaszkodás fehérje (Giap), vagy a Gal/GalNAc lektin. A kontaktus-függő Célsejtek elpusztítása szinte teljesen gátolta a galaktóz vagy GalNAc és célsejtek hiányzik terminális galaktóz-maradékok a felületükön glikoproteinek ellenállnak a trophozoite tapadás és citotoxicitást. Ez arra utal, hogy a Gal/GalNAc lektin fontos virulencia faktor. Ezen túlmenően, a Eh-lektin részt vesz a rezisztencia komplement által közvetített lízist. Mivel a potenciális szerepe tapadás és virulencia és mivel a széklet IgA ellen véd amebic vastagbélgyulladás, a Gal/GalNAc az oltóanyag (Petri és mtsai, 2006, Arch. Med. Res. 37:288).
Az Eh-lektin egy heterodimer, amely egy 170 kDa nehéz láncból és egy 31-35 kDa könnyű lánc diszulfid-kötések. Egy közbenső alegység 150 kDa nem kovalensen kapcsolódó heterodimer. A nehéz lánc egy transzmembrán domént és egy szénhidrát-kötő domént. Minden alegységeket kódolják sokgénes családok. Jelenleg öt tagja a nehéz lánc család, 6-7 tagjai a könnyű lánc család és 30 tagjai a közbenső lánc család. A tagok a nehéz lánc gén család mutatnak 89-95% -os szekvencia azonosságot mutat aminosav szinten, míg a könnyű lánc a családtagok kevésbé konzerváltak megosztását csak 79-85% -os szekvencia azonosságot.
E. dispar is kifejezi Gal/GalNAc lektin a felszínén. Mindkét E. dispar és E. histolytica kell, hogy tartsák a nyálkahártya-réteg, amely gyógyszeres a Gal/GalNAc lektin. A nyálka áll glikoproteinek nevű nyál. Az uralkodó mucin megtalálható a bélnyálkahártya MUC2 amelyet széles körben glikozilált O-kapcsolt GalNAc maradványok. A szekvencia a könnyű és nehéz lánc gének E. dispar homológ, de nem azonos, az említett E. histolytica. Antigén közötti különbségek Giap E. dispar és E. histolytica is leírták, hogy csak két epitópra hatból megoszlik a két faj között (lásd E. dispar). Nem ismert, hogy ezek a szekvencia különbségek felelősek a különbségek virulencia között E. dispar és E. histolytica. Betartása nyilvánvalóan fontos mindkét faj, de lehetséges, hogy tapadást minőségileg vagy mennyiségileg eltérő a két faj között.
[Review az Eh-lektin: Petri et al (2002) Annu. Rev. Microbiol. 56:39.]
Amebaporus. Egy család a pórusképző polipeptidek azonosították E. histolytica és E. dispar. A három családtagok kijelölt amebapore A, B és C amebapore A dominál kifejezve. Az érett polipeptid a 77 aminosav hosszú, és képez dimereket alacsony pH (4-6). Három ilyen dimerek majd össze egy üreges gyűrű alakú struktúra. Ez a hexamer ezután lehet interkalálódni be membránok és bevezetésére 2 nm-es pórusok (azaz lyukak) ami sejthalálhoz vezet. A pórusképző aktivitás függ ezen összeszerelési folyamat kezdve a dimerizációs. Amebabpore A jelentése 95% -ban azonos (azaz négy maradékok egymástól eltérő) között az E. histolytica és E. dispar. Ezen túlmenően, a E. dispar amebapore körülbelül fele a pórusképző aktivitást, mint az E. histolytica amebapore. Ez a különbség a pórusképző aktivitás tulajdonítható a glutamát maradékot 2-es helyzetben a E. histolytica amebapore, összehasonlítva egy prolin maradék a E. dispar amebapore. Ez különösen a aminosavcsoport fontos a kialakulását a dimerek és úgy gondoljuk, hogy a dimerek E. dispar amebapore kevésbé stabilak.
Amebapore lokalizálódik vakuoláris rekeszek (pl, élelmiszer vakuolumok) belül trophozoite és a legaktívabb savas pH arra utal, hogy a fő funkciója amebapore hogy lizálják elfogyasztott baktériumok. Mindazonáltal amebapore játszik, mint egy virulencia faktor, hogy a genetikai manipuláció az E. histolytica így csökkent expressziója amebapore csökkenéséhez vezet a patogenitást (képes formában máj tályogok), valamint csökkentése baktericid aktivitását (Bracha és munkatársai: Mol. Microbiol. 34:363, 1999). Hasonlóképpen, módosított E. histolytica teljesen mentes a amebapore termelés nem alkotnak máj tályogok modell rendszerekben (Zhang és munkatársai, Inf. Imm. 72:678, 2004). Azonban ezek amebas képesek gyulladást okozhatnak, és szövetkárosodások modellek amebic colitis.
[Felülvizsgálata amebapore: Leippe munkatársai, Tr. Parasitol. 21:5, 2005]
A proteázok. A proteázok olyan enzimek, amelyek lebontják más fehérjék, és hozzájárulhat a patogenezis ok E. histolytica. Ebben a tekintetben, az E. histolytica kifejezi és szekretálja a magasabb szintű cisztein-proteázok, egy bizonyos osztálya proteáz, mint az E. dispar. Cisztein-proteázok kimutatták, hogy megzavarják a polimerizációját MUC2, a fő komponens a vastagbél nyálka. Ez leromlott váladék kevésbé hatékonyan blokkolja tapadását trophozoiták a hámsejtek. Destruction az extracelluláris mátrix (ECM) által proteázok is megkönnyíti trophozoite invázió. A cisztein proteázok inhibitorai csökkentheti májtályog méretű kísérleti modelleken.
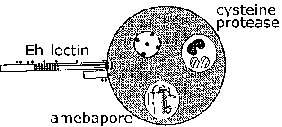
Tényező histolytica vs dispar Eh-lectin szekvencia és epitóp különbségek amebapore Ed kevesebb aktivitást (Pro/Glu) proteázok Eh egyedülálló gének és kifejezi több aktivitást Figura Horstmann és munkatársai (1992) Trop. Med. Parasitol. 43, 213.
Húsz különböző cisztein-proteáz gént azonosítottak E. histolytica. Orthológja két E. histolytica cisztein proteáz gének nem találhatók az E. dispar. Az egyik ilyen, a kijelölt CP5, van kifejezve magas szinten a trophozoite felületre. Mutánsok expresszáló alacsonyabb szintű CP5 volt egy csökkent képessége, hogy a máj tályogok egy hörcsög amebiasis modell. Azonban ezek a mutánsok is volt egy csökkentett növekedési ráta és az alacsonyabb erythrophagocytic aktivitás, így nem világos, hogy CP5 közvetlenül részt vesz a invazivitását E. histolytica. Továbbá gátlása 90% CP5 aktivitás nem befolyásolják az E. histolytica trophozoiták elpusztítani sejt monorétegek in vitro. CP1, CP2, és CP5 a leginkább bőségesen kifejezve cisztein proteázok E. histolytica, mivel CP3 a leggyakoribb E. dispar. Érdekes, hogy több mint kifejezése CP2 E. dispar növelte a képességét trophozoiták elpusztítani sejt monorétegek in vitro. Azonban a több mint kifejezése CP2 nem vezetett a képességét, E. dispar alkotnak máj tályogok futóegér. Ezért nem világos, hogy a pontos szerepeket proteázok játszanak patogenezisében.
Összefoglalva, a patogenezis társított E. histolytica fertőzés elsősorban annak köszönhető, hogy képes támadják szövetek és megölik gazdasejtekben. Több lehetséges virulencia tényezőt azonosítottak (lásd a táblázatot). Ugyanakkor nem világos, hogy pontosan milyen szerepet a különböző virulencia faktorok játszanak a fejlesztés invazív betegség. Az egyik megközelítés, hogy megértsék a patogenezise összehasonlítani ezeket a tényezőket az E. histolytica és E. dispar. Ez a két faj szorosan kapcsolódnak, és a potenciális virulencia faktorok találhatók mindkét faj. Ragaszkodás, citolitikus és proteolitikus aktivitás rejlő biológiai jellemzői a két faj, és ezek a tevékenységek nem feltétlenül vezet a patológia. Vannak azonban olyan kvalitatív és kvantitatív különbségek E. histolytica és E. dispar, amelyek felelősek a különbségek a virulenciát. Ezek a genetikai különbségek E. histolytica és E. dispar azt jelzik, hogy patogenezise részben velejárója a parazitát. Azonban patogenezise oka valószínűleg az együttes hatása számos gazda- és parazita tényezők, valamint a virulencia képviselheti a mértéke, hogy a fogadó szabályozhatja trophozoite invázió és a replikáció.
[Lásd Huston, 2004, Tr. Parasitol. 20:23 vagy Ralston és Petri, 2011, Tr. Parasitol. 27:253 vélemények az patogenezisében.]
KLINIKAI ELŐADÁS
Amebiasis bemutatja széles körű klinikai szindrómák (táblázat), amely tükrözi a lehetséges E. histolytica válik az invazív és okoz egy progresszív betegség. A lappangási idő között lehet néhány nap, hónap vagy év 2-4 héttel a leggyakoribb. Átmenet egyik típusa a bél szindróma egy másik is előfordulhat, és bélfertőzések adhat okot extraintesztinális fertőzések.
Bélbetegségek
Extraintesztinális betegség
|
A legtöbb diagnosztizált egyének E. histolytica (vagy E. dispar) nem mutatnak tüneteket, vagy bizonytalan és nem specifikus hasi panaszok. Ez az állapot akkor is fennállnak, vagy elért egy tüneti fertőzés. Tüneti nondysenteric fertőzések mutatnak változó tünetek az enyhe és átmeneti intenzív és tartós. Jellemző tünetek: hasmenés, hasi görcsök, puffadás, émelygés és étvágytalanság. A hasmenés gyakran váltakozik időszakok székrekedés vagy lágy széklet. Széklet néha tartalmaznak nyálka, de nincs látható vér.
Amebic vérhas általában lassan indul, több napon hasi görcsök, tenezmus, és alkalmi laza széklet, de halad a hasmenés véres és nyákos. Vér, váladék és a darab elhalt szövetek egyre nyilvánvalóbb, hogy a több széklet növekszik (10-20 vagy annál több naponta) és a széklettel gyakran tartalmaznak kis székletet. Néhány betegnél láz, hányás, hasi nyomásérzékenység, vagy kiszáradás (különösen a gyermekek), mint a betegség súlyosságát növeli. Heveny, vagy grangrenous, colitus egy ritka, de igen súlyos formája a bél amebiasis. A betegnél súlyos véres hasmenés, láz, és a diffúz hasi nyomásérzékenység. A legtöbb nyálkahártya van szó, és a mortalitás aránya meghaladja az 50%. A krónikus amebiasis jellemzett ismétlődő támadások vérhas a köztes időszakokban enyhe vagy közepesen súlyos gyomor-bélrendszeri tünetek, akkor is előfordulhat.
Amebomas jelen fájdalmas hasi tömegek leggyakrabban a vakbél és a felszálló vastagbél. Obstruktív tünetek vagy vérzések is társított ameboma. Amebomas ritkák, és lehet összetéveszteni a karcinóma vagy daganatok. Perianalis fekélyek olyan formája, bőr- amebiasis eredő közvetlen terjedése a bél fertőzés.
Amebic máj tályogok leggyakoribb formája extraintesztinális amebiasis. A kezdeti tünetek a máj gyors lehet, vagy fokozatosan. Beszűkült fertőzések jellemzi hepatomegalia, a máj érzékenység, fájdalom a jobb felső negyedben, láz és étvágytalanság. Láz néha előfordul naponta délután vagy este. A májfunkciós vizsgálatok rendszerint normális vagy enyhén rendellenes és sárgaság szokatlan. Máj tályogok időnként betör a hashártya eredményező hashártyagyulladás.
A pulmonális amebiasis általában abból a közvetlen kiterjesztése a máj tályog a membránon keresztül. Klinikai tünetek leggyakrabban a köhögés, mellkasi fájdalom, légszomj (nehézlégzés), és a láz. A köpet lehet gennyes vagy véres, és tartalmaznia trophozoiták. A dús köpködés (azaz Vomica) gennyes anyag is előfordulhat. Elsődleges áttét a tüdőben ritka, de előfordul. Hasonlóképpen, a fertőzés más szervek (pl., Az agy, lép, szívburok) is ritka. Klinikai tünetek kapcsolódnak az érintett szerv.
Külsőleges amebiasis az eredménye a bőr vagy a nyálkahártyák is fürdött folyadékok trophozoiták. Ez a kapcsolat lehet az eredménye, sipoly (bél, máj, a gáti) vagy egy invázió a nemi szervek. Bőrelváltozások egy nedves, szemcsés, elhalt felületet kiemelkedő határok és lehet nagyon romboló hatású. Klinikai diagnózis nehéz, és általában úgy epidemiológiai kockázati tényezők (pl., A veszélyeztetett területeken, a férfi homoszexualitás, stb.)
DIAGNÓZIS, KEZELÉS ÉS ELLENŐRZÉS
|
Diagnózis |
Bélbetegségek
Extraintesztinális (hepatikus) Betegség
|
Végleges diagnózis amebiasis igényli kimutatása E. histolytica ciszták vagy trophozoiták székletben vagy szöveteket. Székletmintát kell őrizni és pácolt és mikroszkópos vizsgálattal. Ciszták általában túlsúlyban kialakított széklet és trophozoiták hasmenéses széklet (lásd morfológia). Friss széklet is azonnal vizsgálni motilis trophozoiták, melyek olyan progresszív motilitás. Sigmoidoscopia felfedi a jellemző fekélyek, különösen a súlyosabb betegség. Aspirációs biopszia vagy is meg kell vizsgálni mikroszkóppal trophozoiták.
E. histolytica és E. dispar nem lehet megkülönböztetni a morfológiai kritériumok. Antigénkimutatás készletek állnak rendelkezésre a pozitív azonosítása e fajok. Az egyik ilyen gyors antigént kimutató vizsgálat az e E. HISTOLYTICA QUIK CHEK (TechLab, Inc).
Szerológia különösen hasznos a diagnózis extraintesztinális amebiasis. Nagyobb, mint 90% -ánál a invazív vastagbélgyulladás és a máj tályogok mutatnak szérum antitestek ellen E. histolytica. Azonban az antitestek évekig és megkülönböztetve a múlt és a jelenlegi fertőzés jelenthet problémát az endémiás területeken. Nem invazív képalkotó technikák (pl., Ultrahang, CT, MRI) lehet használni, hogy érzékeli a máj tályogok. Az is lehetséges, hogy szívja hepatikus tályogok. Ez azonban ritkán kerül sor, és csak jelzett kiválasztott esetekben (pl., Szerológiai és képalkotó nem áll rendelkezésre, a terápiás célokra). A felszívott rendszerint sűrű vörösesbarna folyadékot, ritkán tartalmaz trophozoiták. Trophozoiták legvalószínűbben megtalálható a tályog fala, és nem a nekrotikus törmelék a tályog központban.
Számos gyógyszer áll rendelkezésre kezelésére amebiasis és a kiválasztott gyógyszer (ek) függ a klinikai szakaszában a fertőzés (táblázat). A prognózis kezelést követően általában jó szövődménymentes esetekben. Olyan esetekben, amikor az E. histolytica megerősítik vagy a faj (azaz dispar vagy histolytica) ismeretlen, tünetmentes ciszta járókelők kell kezelni, hogy megakadályozzák a progresszió a betegség súlyos, és hogy ellenőrizzék a betegség terjedését. Azonban sok endémiás területeken, ahol az arányok az újrafertőződés magasak, és a kezelés drága, a standard gyakorlat az, hogy csak kezelésére tüneti esetben. Metronidazol vagy tinidazolt (ha van) ajánlott minden tüneti fertőzések. Ezt a kezelést meg kell majd vagy kombinálható lumen antiamebic gyógyszerek leírtak tünetmentes.
Amebiasis kezelés |
||||||||
|
Azokban az esetekben, fulmináns amemic colitis vagy perforáció a bélfal egy széles spektrumú antibiotikum is használható kezelésére bélrendszeri baktériumok a hashártya. Nekrotikus colitis sürgős kórházi helyreállítani a folyadék- és elektrolit-egyensúly. Ezen túlmenően, emetin vagy dehydroemetine néha együtt adagolnak a nitro-imidazol. Ez csak akkor történik a legsúlyosabb esetekben, toxicitása miatt ezeknek a gyógyszereknek. Műtét is szükség lehet, hogy lezárja perforációkkal vagy egy részleges colostomia. Tályog elvezetése májeltérések (azaz aspirációs vagy sebészeti vízelvezetés) ma már ritkán végzett terápiás célokra, és csak abban az esetben jelzi a nagy tályogok nagy valószínűséggel a szakadás.
Megelőzési és ellenőrzési intézkedések hasonlóak más betegségek által továbbított széklet-szájon (lásd Kockázati tényezők vagy azok tárgyalása Giardia kontroll). A fő különbség az, hogy az ember az egyetlen gazda az E. histolytica, és nincs lehetősége zoonózis átvitel. Ellenőrző alapul elkerülve a szennyeződése élelmiszer vagy víz székletanyag. Egészségügyi oktatás tekintetében javítja a személyes higiénia, egészségügyi ártalmatlanítása széklet, és kézmosás különösen hatásos. Eredetű szennyeződés csökkenti endémiás és járványok. Mint Giardia, Entamoeba ciszták ellenálló a standard klór kezelés, de megölte jód vagy forrásban. Ülepítés és szűrés folyamatok meglehetősen hatékonyan eltávolítja Entamoeba ciszták. Kemoprofilaxis nem ajánlott.
Vélemények az amebiasis:
- Haque, R. et al (2003) Amebiasis. N. Engl. J. Med. 348:1565.
- Stanley, S.L. (2003) Amoebiasis. The Lancet 361:1025.
BLASTOCYSTIS HOMINIS
Blastocystis hominis egy közös szervezet megtalálható az emberi széklet. Mivel a kezdeti leírás körülbelül 100 évvel ezelőtt, azt már változóan minősül ameba, egy élesztő, egy spórás és a ciszta szakaszában egy ostoros. Elemzés a kis alegység-rRNS-szekvencia azt mutatja, hogy Blastocystis legszorosabban összefügg a stramenopiles, egy komplex együttesét egysejtű és muticellular egysejtűek. Egyéb stramenopiles közé kovamoszatok, barna alga, és a víz formák. Sok a jellemzőit Blastocystis ismeretlen vagy vitatott. Az átviteli mód, mechanizmusa sejtosztódást, és egyéb jellemzőit az életciklus nem meggyőzően bizonyított. Hasonlóképpen, az állapot Blastocystis mint egy patogén, kommenzalista, vagy opportunista organizmus ismeretlen.
Blastocystis polimorf, hogy a különböző morfológiai formákban találhatók ürülék és in vitro kultúrában.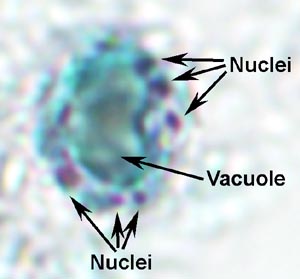
Voltak több információ van arra Blastocystis betegséget okoz, valamint számos jelentés utal az ellenkezője. Hasmenés, görcsök, émelygés, hányás, hasi fájdalom összefüggésbe hozták a nagyszámú organizmusok a székletben. Ezen túlmenően, néhány tanulmány kimutatta, hogy a kezelés enyhíti a tüneteket, és törli a szervezetekre. Azonban a gyógyszerek ellen Blastocystis (pl. Metronidazol) is működnek ellen sok más bélrendszeri protozoonok és baktériumok. Az képtelenség, hogy zárja ki más élőlények, mint a forrás, a tünetek és a megfigyelés, hogy sok a fertőzött személyek nem mutatnak tüneteket megnehezíti felhívni végleges következtetéseket patogenezise Blastocystis. Továbbá lehet, hogy Blastocystis elsősorban commensal, de mutathat virulencia mellett specifikus gazda feltételek, mint az egyidejű fertőzések, a rossz táplálkozás, vagy immunszuppresszió.
Blastocystis is megtalálható számos állatok, beleértve az emlősöket, madarak, hüllők, kétéltűek és még rovarok, és mutat számos molekuláris diverzitás. Közötti genetikai távolság Blastocystis izolátumok nagyobb, mint a genetikai távolság között az E. histolytica és E. dispar (lásd a tárgyalást az E. dispar). Ez megnehezíti a kijelölését fajok és történelmileg humán izolátum már kijelölt B. hominis és elkülöníti az egyéb gazdaszervezetek, mint Blastocytis sp. Azonban filogenetikai elemzés azt mutatja, hogy nincsenek kizárólag emberi kládok és humán izolátumok találhatók mind a kládok. Ez felveti annak lehetőségét, hogy Blastocystis nem fogadó specifikus, és lehet továbbítani zoonotically. Ezen túlmenően, a széles körű genetikai diverzitás megmagyarázhatja a vita vonatkozó pathogenecity az Blastocystis, hogy egyes genotípusok lehetnek virulens, mint mások. A vizsgálatok azonban e kérdés arra utalnak, hogy nem ez a helyzet. Állásfoglalás a zavart a taxonómia, az átviteli és virulencia Blastocystis lesz szükség további vizsgálatok.
Vélemények az Blastocystis:
- Clark CG, van der Giezen M, Alfellani MA, Stensvold CR (2013) Recent Developments in Blastocystis Research. Advances in Parasitology 82, 1-32.
- Scanlan PD (2012) Blastocystis: past pitfalls and future perspectives. Trends in Parasitology 28, 327-334.
- Tan KSW, Mirza H, Teo JDW, Wu B, MacAry PA (2010) Current Views on the Clinical Relevance of Blastocystis spp. Current Infectious Disease Reports 12, 28-35.
NEM PATOGÉN KOMMENZÁLIS
Számos protozoa, tartózkodhat a gyomor-bél traktus az emberek. A legtöbb ilyen mutatnak alig vagy egyáltalán nem nyilvánvaló patológia. Fertőzés ezekkel protozoonok bizonyítéka széklet szennyeződés és kockázatot jelez több súlyos fertőzések, mint például Giardia vagy E. histolytica. Ezek a nem kórokozó fajok is szabad összetéveszteni a potenciálisan patogén Giardia vagy E. histolytica és az eredmény a felesleges gyógyszeres kezelést. Ezen túlmenően, egy ilyen téves diagnózis is problémás, hogy a valódi oka a tünetek a nem fogadott és a megfelelő kezelést késni fog.
• E. histolytica
• E. dispar
• E. coli
• E. hartmanni
• E. polecki
• E. gingivalis
• Egyéb Entamoeba
• Egyéb Bél Amebae
• Egyéb Bél ostorosok
• Blastocystis
Entamoeba embert is fertőző alfaj
Több Entamoeba faj megfertőzni embereket (doboz). E. histolytica okozhat súlyos bélrendszeri betegség jellemző vérhas, valamint egy invazív betegség, amely elsősorban a májban (lásd: Amebiasis). E. dispar morfológiailag azonos az E. histolytica, de nem termel invazív betegség (lásd további vitát E. dispar). A megkülönböztető jellemzője az Entamoeba van nukleáris morfológia ami le, ahol a perifériás kromatin és egy kis karyosome. E. histolytica/dispar, E. coli, és az E. hartmanni lehet megkülönböztetni a méret és a kisebb morfológiai különbségek (lásd táblázat).
| A bél Entamoeba faj | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
*=E. histolytica; **invazív E. histolytica lehet > 20 mm |
Az E. coli, a legnagyobb és a legjobb különböztetni 8 sejtmagok az érett ciszta. A trophozoiták E. coli nehezen lehet megkülönböztetni a E. histolytica/dispar, mivel van némi átfedés a méret tartományban. E. hartmanni meglehetősen hasonlít az E. histolytica, és a korábban a “kis faj” E. histolytica. Általában 10 lm választjuk a határ közötti E. histolytica és E. hartmanni.
E. polecki rendszerint együtt jár a sertés és a majmok, hanem az emberi eseteket néha dokumentáltak. Úgy tűnik, hogy földrajzilag korlátozódik meghatározott területeken, mint egy Pápua Új-Guinea. A trophozoiták hasonló az E. coli, kivéve egy kicsit kisebb, a ciszták hasonlóak E. histolytica, kivéve, hogy az érett ciszta van egy magja.
E. gingivalis nyerhetjük ki a lágy fogkő fogak közötti és mutat hasonló morfológiát az E. histolytica, kivéve, hogy az nem ciszta szakaszban. E. gingivalis ból is szaporodnak a hörgők nyálka, és így jelenik meg a köpet. Ebben az esetben össze lehet keverni az E. histolytica egy tüdő tályog. E. gingivalis trophozoiták gyakran tartalmaznak elfogyasztott leukociták, amely felhasználható, hogy megkülönbözteti a E 8bzrurc. histolytica. A trophozoiták leggyakrabban kinyerjük betegek periodontális betegség, de az etiológia között az organizmus és a betegség még nem állapították meg, és az E. gingivalis kell tekinteni, nem patogén.
Egyéb Bél Amebae
Egyéb, nem patogén amebae közé Endolimax nana és Iodoamoeba bütschlii. Történelmileg, Dientamoeba fragilis már csoportosítva a ameba, de elektronmikroszkóppal és molekuláris filogenetika azt sugallja, hogy ez valójában egy ostoros, és szorosan kapcsolódik a trichomonádok (lásd fent). Mindhárom organizmusok mutatnak hasonló morfológiával és magok, amelyek nem rendelkeznek a perifériás kromatin és egy nagy karyosome. Kisebb morfológiai különbségek lehetővé teszik ezen mikroorganizmusok meg kell különböztetni (táblázat).
| Egyéb Bél Amebae | |||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
*A ostoros esetleg kapcsolódó trichomonádok. |
Egyéb Bél ostorosok
Négy további nem-patogén ostoros visszanyert emberi széklet: Trichomonas hominis, Chilomastix mesnili, Enteromonas hominis és Retortamonas intestinalis. Ezek közül a T. hominis, más néven Pentatrichomonas hominis, a leggyakoribb, és gyakran kinyerjük hasmenéses széklet. Ezek ostoros mutatnak hasonló morfológiájú (táblázat), és nehezen lehet megkülönböztetni. A trophozoiták az összes ilyen ostoros kissé csepp alakú, és tartalmaz egy mag, és a ciszta általában kissé megnyúlt vagy ovális.
| Egyéb Bél ostorosok | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||